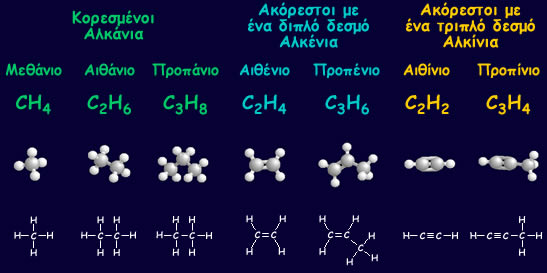
Στον παρακάτω πίνακα δίνονται τα ονόματα, οι μοριακοί και οι συντακτικοί τύποι, καθώς και τα προσομοιώματα των μορίων μερικών υδρογονανθράκων.
Θα παρατήρησες, σίγουρα, ότι στους κορεσμένους υδρονάνθρακες, που καλούνται και αλκάνια, το πλήθος των υδρογόνων είναι διπλάσιο αυτού του άνθρακα + 2.
Στους ακόρεστους με ένα διπλό δεσμό, που καλούνται και αλκένια, διπλάσιο και σε αυτούς με ένα τριπλό δεσμό, που καλούνται και αλκίνια, ίσο με το πλήθος των ατόμων του άνθρακα - 2.
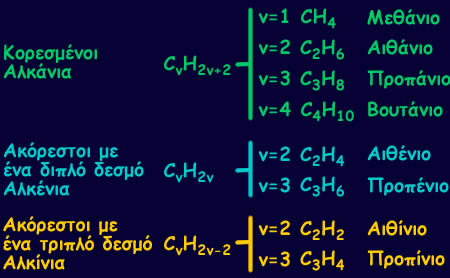
Οι γενικοί κανόνες για το πλήθος των ατόμων άνθρακα και υδρογόνου στους υδρογονάνθρακες εκφραζονται με τους εμπειρικούς ή γενικούς τύπους. Από αυτούς προκύπτουν εύκολα οι μοριακοί τύποι όλων των υδρογονανθράκων, αν αντικαταστήσουμε σε αυτούς την τιμή του "ν".
Έτσι, ο κορεσμένος υδρογονάνθρακας με 4 άτομα άνθρακα, το βουτάνιο, έχει μοριακό τύπο: C 4 H 10 (ν=4).
Όσο για τα ονόματα, μετά το βουτάνιο, είναι το πεντάνιο, το εξάνιο, το επτάνιο, το οκτάνιο, κ.λπ.